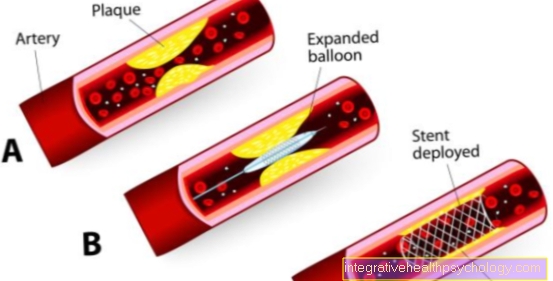
Biologics
introduktion
Immunsystemet er essentielt for overlevelse af ethvert menneske. I løbet af udviklingen har dette udviklet sig til det såkaldte adaptive immunsystem hos mennesker. Dette giver os muligheden for at reagere mere forskelligt og mere effektivt på bakterier og vira. Immunsystemet beskytter os. Det hjælper os med at overleve kampen med betændelse bedre. Der er mange forskellige typer af inflammationsmodulatorer. For eksempel den såkaldte tumor nekrose faktor-alfa, der er forkortet til TNF-a. Sammen med andre faktorer sikrer dette, at inflammatoriske celler og tumorceller fjernes, før de kan udløse sygdomme.

Men disse "livvagter" i vores krop kan også blive "kriminelle". Fordi nogle gange vender vores immunsystem mod os. I disse tilfælde udvikles autoimmune sygdomme, der er vanskelige at behandle med medicin. Det er her biologi kommer ind. Biologi kaldes også biofarmaceutiske midler eller biofarmaceutiske midler. Dette er lægemidler, der produceres i genetisk modificerede organismer ved hjælp af forskellige metoder til bioteknologi. Eksempler på disse lægemidler er såkaldte "monoklonale antistoffer" eller såkaldte "fusionsproteiner". TNF-a-hæmmere, blandt dem TNF-alfa-receptorantagonister, tilhører denne gruppe af lægemidler.
En velkendt biologisk er adalimumab, også kendt under handelsnavnet Humira.
Indikationer
TNF-a-receptorantagonister bruges i inflammatoriske, kroniske autoimmune sygdomme. Dette betyder, at de er indiceret til alle sygdomme, hvor kroppens eget immunsystem kæmper mod kroppen i stedet for at kæmpe for det. I denne proces spiller TNF-a ofte en vigtig rolle. Det sikrer, at visse celler begynder at opføre sig som såkaldte fjernereceller (makrofager) og dermed ødelægge væv, knogler, brusk og, afhængigt af sygdommen, andre kropsceller.
Specifikke indikationer er for eksempel reumatoid arthritis, såkaldt juvenil idiopatisk arthritis, psoriasisarthritis, plaque psoriasis, ankyloserende spondylitis, Crohns sygdom eller ulcerøs colitis. Biologiske medikamenter, såsom TNF-a-receptorantagonister, bruges, når ingen andre lægemidler hjælper med de nævnte sygdomme eller forårsager for mange bivirkninger.
Biologi til ankyloserende spondylitis
Bechterews sygdom er en inflammatorisk, kronisk autoimmun sygdom. Det hører til den reumatiske gruppe af former. Det er en af de såkaldte spondylarthritis. Ved Bechterews sygdom er kroppens eget immunsystem rettet mod knogler og bruskceller i bækken- og rygområdet og ødelægger dem. Dette kan føre til ledssmerter og deformiteter i de tilsvarende områder af kroppen. Under visse omstændigheder kan TNF-a-receptorantagonister også anvendes. De hæmmer messenger-stoffet TNF-α. Da dette messenger-stof spiller en vigtig rolle i den inflammatoriske proces, blokeres sygdomsprocessen af TNF-a-inhiberingen. Dette kan lindre symptomerne og forsinke udviklingen af sygdommen.
Læs mere om emnet på: Terapi af ankyloserende spondylitis
Biologi til psoriasis
Den kolokiale psoriasis er kendt i teknisk jargon som plaque psoriasis. Det manifesterer sig som svær fladning af huden med kløe og brændende smerter. Det kan forekomme i forskellige sværhedsgrader. I tilfælde af moderat til svær alvorlighed anvendes TNF-a-receptorantagonister undertiden.
Man taler om denne sværhedsgrad af sygdommen, når mere end 10% af hudoverfladen påvirkes, eller hudforandringer dukker op i særligt synlige dele af kroppen, såsom hænder eller ansigt. Et meget højt lidelsesniveau fra patientens side er også et kriterium for klassificering af moderat til svær psoriasis. I nogle tilfælde kan de biologiske stoffer allerede anvendes, uden at alle andre aktive ingredienser er slået fejl, eller at tilstedeværelsen af bivirkninger skal bevises. TNF-a-receptorantagonisterne kan bremse de inflammatoriske reaktioner på det sted, hvor de opstår, og dermed forbedre livskvaliteten for den berørte patient.
Derudover kan sekundære sygdomme, der kan være resultatet af psoriasis, såsom depression, i et vist omfang forebygges.
Læs mere om emnet på: Psoriasis eller psoriasis behandling
Biologi mod ulcerøs colitis
Ulcerøs colitis er kendetegnet ved stærk inflammatorisk, kronisk, intermitterende processer i tarmslimhinden og det underliggende bindevævslag. I alvorlige tilfælde dannes mavesår. I modsætning til Crohns sygdom påvirkes tyktarmen næsten udelukkende. Også i denne type autoimmun sygdom kan TNF-a-receptorantagonister påvirke sygdommens forløb positivt. En række forskellige biologiske stoffer er nu godkendt til behandling af ulcerøs colitis.
Læs mere om emnet på: Terapi med ulcerøs colitis
Biologi mod Crohns sygdom
Crohns sygdom er en kronisk inflammatorisk autoimmun sygdom. Kroppens eget forsvarssystem er rettet mod celler i fordøjelseskanalen. Dette kan påvirke hele fordøjelsessystemet fra mundhulen til anus. Her spiller TNF-a en rolle ved, at det sikrer, at inflammatoriske processer og celleødelæggelse forekommer. Derfor kan TNF-a-hæmmere også bremse sygdomsprocesserne i sammenhæng med Crohns sygdom og delvist forhindre følgeskader.
Læs mere om emnet på: Terapi mod Crohns sygdom
Biologi til gigt
Mange sygdomme er reumatiske. Når reumatisme anvendes fælles, er det normalt reumatoid arthritis. Dette er en kronisk inflammatorisk autoimmun sygdom, hvor immunceller ødelægger brusk og knogler. Der er ledsmerter og hævelse. Dette sker ofte i området med fingrene og tæerne i metatarsophalangeal led. Typisk morgenstivhed forekommer ofte. Også her spiller inflammationsmodulatoren TNF-a en vigtig rolle. TNF-a-receptorantagonister kan bruges i reumatoidbehandling, hvis andre foranstaltninger mislykkes.
Læs mere om emnet på: Terapi af reumatoid arthritis
Aktiv ingrediens / virkning
De fleste biologikas er proteiner. Der er forskellige generationer af biologik og derfor også af TNF-a-hæmmere. Generationer adskiller sig fra fremstillingen.
Afslutningen af navnet afslører, hvor meget museprotein der stadig findes i de aktive ingredienser. Med afslutningen –omab er det 100%, med slutningen –ximab er der 25% museprotein, med slutningen - 5-10% er stadig tilgængelig og med slutningen –umab overhovedet ikke. Dette spiller en rolle i medicinenes tolerabilitet.
Derudover kan TNF-a-hæmmere arbejde på forskellige måder. De kan opfange TNF-a og således forhindre, at det binder til dets receptor. Som et resultat finder visse processer i cellen, der vil føre til den destruktive immunreaktion, ikke sted.En anden mulighed er, at TNF-a-inhibitoren blokerer bindingsstedet for TNF-a til receptoren. Lægemidlet fungerer derefter som en såkaldt antagonist. Det er også muligt, at TNF-a-hæmmere fungerer som såkaldte fusionsproteiner. Disse kaldes også lokke-receptorer. Fluoreceptorer er receptorer, der binder ligander, men ikke transmitterer signaler. TNF-a-decoy-receptorer er opløselige receptorer, der opfanger TNF-a, før den har nået sin oprindelige destination. Som et resultat er der ikke længere noget signal, og væksten af de destruktive immunceller bremses.
Enbrel®
Den aktive ingrediens Etanercept er til stede i det kommercielle præparat Enbrel®. Det er en såkaldt lokkemiddelreceptor eller fusionsprotein. Enbrel® bruges især til reumatisk arthritis, juvenil kronisk arthritis, psoriasisartrit og såkaldt spondylarthritis. Psoriasisgigt er en speciel form for psoriasis, der er forbundet med ledsmerter. Enbrel® fungerer som en TNF-a-hæmmer ved disse sygdomme såvel som i nogle andre autoimmune sygdomme. Enbrel® er imidlertid ikke effektiv til Crohns sygdom. Som regel administreres det subkutant en gang om ugen med 50 mg eller to gange om ugen med 25 mg.
Læs mere om emnet på: Enbrel®
Remicade®
Den aktive ingrediens infliximab findes fx i det kommercielle præparat Remicade®. Infliximab er et kimært monoklonalt antistof, der blokerer for aktiviteten af TNF-a. Da det er et kimært monoklonalt antistof, er den vigtigste rygrad human og antigenbindingsstederne (25%) er museprotein. Dette betyder, at effektiviteten er højere end med såkaldte murine monoklonale antistoffer, der består af 100% museprotein og lavere sammenlignet med humaniseret (5-10% museprotein) eller humane monoklonale antistoffer (0% museprotein). Følgelig er risikoen for allergier og intolerance lavere end med murine monoklonale antistoffer og højere end med humaniserede eller humane antistoffer. Remicade® bruges til reumatoid arthritis, psoriasisartrit, ankyloserende spondylitis og andre autoimmune sygdomme. I modsætning til etanercept er den aktive ingrediens infliximab også effektiv ved Crohns sygdom. Doseringen er 3-5 mg pr. Kg kropsvægt, afhængigt af sygdommen.
dosering
Da bilogikas normalt er proteiner, skal de gives parenteralt (via en infusion). Oral indtagelse er ikke mulig, fordi kroppen derefter ville fordøje den, og de aktive ingredienser ikke kunne udvikle deres virkning. Doseringen afhænger af den aktive ingrediens og den tilstedeværende sygdom. Dosis er normalt i et til to-cifret milligram område og administreres 1-2 gange om ugen.
pris
Omkostningerne ved biologika er meget høje. Derfor bruges de for det meste kun som en sidste udvej. Det vil sige, hvis alle andre aktive ingredienser, der er indikeret for de respektive sygdomme, ikke har succes. Som regel koster to sprøjter omkring 1.600 euro om måneden.
Bivirkninger
Under specialistbehandling og -observation er TNF-a-blokkere relativt godt tolererede og sikre lægemidler. Som med ethvert lægemiddel kan der dog forekomme bivirkninger. Bivirkningerne kan opdeles i dem, der er relateret til applikationen, og dem, der er relateret til interferens med immunsystemet. Da biologien skal gives parenteralt (som en infusion), kan teoretisk opstå infusionsreaktioner. Sammenlignet med anden biologi, sker dette oftere med den aktive ingrediens infliximab. Men med specialbehandling kan disse typer bivirkninger normalt kontrolleres godt. Hvis Biologikas gives subkutant (under huden), kan lokale hudreaktioner udløses. Imidlertid har seponeringen af behandlingen hidtil været meget sjældent nødvendigt.
Bivirkninger, der opstår som et resultat af interferens med immunsystemet, er baseret på den yderligere undertrykkelse af fysiologiske processer i vores krop. Messenger-stoffet TNF-α er faktisk en vigtig inflammationsmodulator. Selv hvis det delvis er rettet mod immunsystemet, har det vigtige opgaver i forbindelse med immunsystemet. Hvis disse vigtige funktioner af TNF-α blokeres permanent af medikamenter, kan dette føre til tilsvarende bivirkninger. Modtageligheden for infektioner kan øges, og risikoen for kræft kan muligvis også stige ved langtidsbrug. Der kan forekomme skader på leveren, nyrerne og hjertet. Derudover kan TNF-a-hæmmerne genaktivere inaktiv tuberkulose og herpes zoster.
Afhængig af hvilken generation af monoklonale antistoffer det er, er risikoen for intolerance og allergier højere eller lavere. Dette betyder, at jo mere museprotein der stadig findes i den aktive ingrediens, jo større er risikoen for allergi og intolerance. Derudover kan visse autoantistoffer forekomme. Behandling med en TNF-a-hæmmer resulterede sjældent i det, der er kendt som lupus erythematosus. Dette faldt også igen, når biologien blev afbrudt. Derudover er forskellige sygdomme og tilbagefald i forbindelse med multipel sklerose samt forværring i tilfælde af udtalt hjerteinsufficiens blevet beskrevet.
interaktion
Hvis der gives vaccinationer med levende vacciner og på samme tid TNF-α-hæmmere, kan dette udløse sygdom med vaccinepatogenet i stedet for en vaccinationseffekt. Desuden kunne en interaktion observeres, når to biologiske lægemidler kombineres. For eksempel er dette blevet observeret ved samtidig indgivelse af etanercept og anakinra i løbet af behandlingen af reumatoid arthritis. Effekten blev ikke forbedret, men bivirkningerne blev styrket. Der udviklede sig alvorlige infektioner og en mangel på visse blodlegemer, så hvad der kaldes neutropeni udviklede sig.
Hvornår bør biologi ikke tages?
Hvis der er en tidligere tuberkulosesygdom, skal der ikke anvendes nogen TNF-a-hæmmere. Dette er uanset hvor længe siden du havde tuberkulose. Dette skyldes det faktum, at inaktiverede tuberkulosebakterier stadig er til stede i kroppen, efter at nogen har lidt af tuberkulose. Disse tuberkulosebakterier er inaktive, fordi såkaldte makrofager holder øje med dem. De passe på, at bakterierne ikke bliver aktive igen. For at makrofagerne skal være i stand til at udføre denne opgave, har de brug for TNF-α. Hvis dette ikke længere er tilstrækkeligt tilgængeligt for makrofagerne på grund af lægemidlets virkning, kan de ikke længere udføre deres opgave. Som et resultat kan tuberkulosebakterierne blive aktive igen og genaktivere tuberkulose.
Derudover er tilstedeværelsen af hepatitis B en kontraindikation til behandling med et biologisk middel. Det har vist sig, at i dette tilfælde kan behandling med en TNF-a-hæmmer genaktivere herpes zoster. Dette manifesterede sig i en øget forekomst af helvedesild og skoldkopper hos voksne.
Der blev imidlertid fundet forskelle i de forskellige aktive ingredienser i TNF-a-hæmmerne. Sygdommene forekom hyppigere hos patienter, der blev behandlet med infliximab, mens disse bivirkninger næppe kunne ses i terapi med etanercept. Risikoen for reaktivering korrelerede med alderen i begge sygdomme, med såkaldt komorbiditet (yderligere sygdomme) og med yderligere behandling med glukokortikoider, såsom kortison.
For at beskytte patienten er det imidlertid i øjeblikket tilfældet, at behandling med en TNF-a-hæmmer generelt ikke er tilladt i tilfælde af tidligere tuberkulose eller hepatitis B.
Biologi og alkohol - er de kompatible?
Når du behandler med biologiske stoffer, behøver du ikke undvære alkohol fuldstændigt. Der er dog erfaringsrapporter, hvor intolerancer er beskrevet. Da biologik påvirker nyrenes og leverens funktioner, er det meget muligt, at alkoholforbrug kan føre til akut intolerance. Derudover kan langvarigt alkoholforbrug i kombination med biologiske lægemidler øge risikoen for lever- og nyresygdom.
Behandlingsomkostninger
Omkostningerne er meget høje på grund af fremstillingsprocessen og den parenterale administration. TNF-a-hæmmere koster omkring 40.000 til 50.000 euro om året. En enkelt applikation er mindst i det øverste tocifrede interval. Derudover er der personaleomkostninger, udgifter til forundersøgelser osv. Hvis en specialist i en praksis eller på en klinik skulle beslutte, at behandling med en biologisk er den bedste form for terapi, skal han give en god grund til dette. Han kan indsende en ansøgning til sundhedsforsikringsselskabet om at dække omkostningerne. Behandlingen af ansøgningen tager normalt et par uger. Når ansøgningen er kontrolleret, behandlet og godkendt, betaler sundhedsforsikringsselskabet omkostningerne. Det kan dog begrænse varigheden af overtagelsen. Et omkostningsforpligtelse foretages ofte oprindeligt i 3 måneder. Derefter skal en ny ansøgning indgives.
I 2016 blev de første såkaldte biosimilærer til behandling af gigtssygdomme officielt godkendt. Som navnet antyder, svarer de til Biologikas, men ikke det samme som originalen. Nogle forfattere antyder, at de er et billigere alternativ til biologien. Det er kontroversielt, om deres virkning faktisk svarer til originalen. Sundhedsforsikringerne håber at spare milliarder i omkostninger. Andre eksperter er skeptiske over for estimaterne. Indtil videre er biosimilærerne kun blevet brugt hos ca. 1-2% af gigtspatienter. Biosimilærerne anbefales af det tyske selskab for reumatologi. Hun fraråder dog at skifte fra original til erstatningsprodukt. Da der endnu ikke er foretaget langtidsundersøgelser herom, kan specialistforeningen endnu ikke byde en ændring i aktive ingredienser på denne måde velkommen. Hun fraråder kun at træffe sådanne beslutninger af hensyn til omkostningerne. Derudover er hun for optimistisk med hensyn til vurderingen af omkostningsbesparelser. I sammendraget kan det siges, at det endnu ikke er muligt at estimere, hvordan brugen af biologik ser ud i fremtiden på trods af omkostningerne.







.jpg)