Enzymer
definition
Enzymer er kemiske stoffer, der findes overalt i kroppen. De sætter kemiske reaktioner i bevægelse i kroppen.
historie
Ordet enzym blev lavet af Wilhelm Friedrich Kühne 1878 og stammer fra det græske sammensatte ord enzymon, som betyder gær eller surdej. Dette fandt derefter vej ind i international videnskab. Det international union af ren anvendt kemi (IUPAC) og International Union of Biochemstry (IUBMB) udarbejdede en nomenklatur for enzymerne, der definerer repræsentanterne for denne store gruppe af stoffer som en fælles gruppe. Navngivningen, der klassificerer enzymerne efter deres opgaver, er vigtig for at bestemme de enkelte enzymers opgaver.
Illustration af enzymer
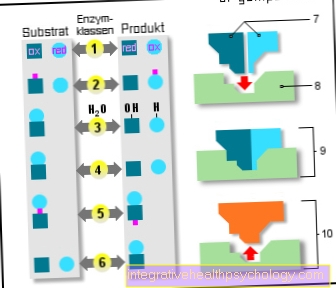
Enzymer
6 enzymklasser:
- Oxidoreduktaser
(Oxidation / reduktion) - Overførsler
(Smitte) - Hydrolaser
(Brug af vand) - Lyaser
(Spaltning) - Isomeraser
(samme empiriske formel) - Ligaser
(Additionsreaktioner) - Underlag
- Aktivt center
- Enzym / substrat
kompleks - Enzym / produkt
kompleks
En oversigt over allebillederne af Dr-Gumpert kan findes på: medicinske illustrationer
Navngivning
Det Navngivning enzymet er tændt tre grundlæggende principper baseret. Enzymnavne, der ender på –ase, beskriver flere enzymer i et system. Selve enzymnavnet beskriver den reaktion, som enzymet sætter i bevægelse (katalyseret). Enzymnavnet er også en klassifikation af enzymet. Derudover et kodesystem, der EF-nummersystem, hvor enzymerne fremstilles under en numerisk kode fire tal kan findes. Det første tal angiver enzymklassen. Lister over alle opdagede enzymer sikrer, at den angivne enzymkode kan findes hurtigere. Selvom koderne er baseret på reaktionens egenskaber, som enzymet katalyserer, viser det sig i praksis, at numeriske koder er uhåndterlige. Systematiske navne baseret på ovenstående regler bruges oftere. Problemer med nomenklaturen opstår for eksempel med enzymer, der katalyserer flere reaktioner. Derfor er der nogle gange flere navne på dem. Nogle enzymer har trivielle navne, der ikke indikerer, at det nævnte stof er et enzym. Da navnene traditionelt er blevet udbredt, er nogle af dem blevet bevaret.
Klassificering efter enzymfunktion
Ifølge IUPAC og IUBMB er enzymer opdelt i seks enzymklasser i henhold til reaktionen, de satte i gang:
- Oxidoreduktaser
Oxidoreductases sætter redoxreaktioner i gang. I denne kemiske reaktion overføres elektroner fra den ene reaktionspartner til den anden. Et stof frigiver elektroner (oxidation), og et andet stof accepterer elektroner (reduktion).
Formlen for den katalyserede reaktion er A ?? + B? A? + B?.
Stof A frigiver en elektron (?) Og oxideres, mens stof B absorberer denne elektron og reduceres. Dette er grunden til, at redoxreaktioner også kaldes reduktionsoxidationsreaktioner.
Mange metaboliske reaktioner er redoxreaktioner. Oxygenaser overfører et eller flere iltatomer til deres substrat. - Overførsler
Transferaser overfører den funktionelle gruppe fra et substrat til et andet. Funktionelle grupper er atomiske grupper i organiske forbindelser, der i vid udstrækning bestemmer stoffets egenskaber og reaktionsadfærd. Kemiske forbindelser, der har de samme funktionelle grupper, er grupperet i stofklasser på grund af deres lignende egenskaber. Funktionelle grupper opdeles efter, om de er heteroatomer eller ej. Heteroatomer er alle atomer i organiske forbindelser, der hverken er kulstof eller brint.
F.eks .: -OH -> hydroxylgruppe (alkoholer) - Hydrolaser
Hydrolaser opdeler bindingerne i reversible reaktioner ved hjælp af vand. Estere, estere, peptider, glycosider, syreanhydrider eller C-C-bindinger. Ligevægtsreaktionen er: A-B + H2O? A-H + B-OH.
Et enzym, der hører til gruppen af hydrolaser, er fx alfa-galactosidase. - Lyaser
Lyaser, også kaldet synthaser, katalyserer spaltningen af komplekse produkter fra enkle substrater uden at opdele ATP. Reaktionsskemaet er A-B → A + B.
ATP er adenosintriphosphat og et nukleotid, der består af triphosphatet af nukleosidet adenosin (og som sådan en energirig byggesten for nukleinsyren RNA). Imidlertid er ATP hovedsagelig den universelle form for øjeblikkeligt tilgængelig energi i hver celle og på samme tid en vigtig regulator for energiforsyningsprocesser. ATP resyntes om nødvendigt fra andre energilagre (kreatinfosfat, glykogen, fedtsyrer). ATP-molekylet består af en adeninrest, sukkerribosen og tre fosfater (? To?) I ester (?) Eller anhydridbindinger (? Og?). - Isomeraser
Isomeraser fremskynder den kemiske omdannelse af isomerer. Isomerisme er forekomsten af to eller flere kemiske forbindelser med nøjagtigt de samme atomer (samme empiriske formel) og molekylvægte, som dog adskiller sig i forbindelsen eller det rumlige arrangement af atomerne. De tilsvarende forbindelser kaldes isomerer.
Disse isomerer adskiller sig i deres kemiske og / eller fysiske og ofte også i deres biokemiske egenskaber. Isomerisme forekommer primært med organiske forbindelser, men også med (uorganiske) koordineringsforbindelser. Isomerismen er opdelt i forskellige områder. - Ligaser
Ligaser katalyserer dannelsen af stoffer, der er kemisk mere komplekse end de anvendte substrater, men i modsætning til lyaser er de kun enzymatisk effektive med ATP-spaltning. Dannelsen af disse stoffer kræver derfor energi, som opnås ved opdeling af ATP.
Nogle enzymer er i stand til at katalysere flere, undertiden meget forskellige, reaktioner. Hvis dette er tilfældet, tildeles de flere enzymklasser.
Du kan også være interesseret i disse artikler:
- Alfa-glucosidase
- Lipase
- Trypsin
Klassificering efter enzymstruktur
Næsten alle enzymer er proteiner og kan klassificeres ud fra længden af proteinkæden:
- Monomerer
Enzymer, der kun består af en proteinkæde - Oligomerer
Enzymer, der består af flere proteinkæder (monomerer) - Multi-enzym kæder
Flere aggregerede enzymer, der samarbejder og regulerer hinanden. Disse enzymkæder katalyserer de successive trin i cellens metabolisme.
Derudover er der individuelle proteinkæder, der indeholder flere enzymaktiviteter; disse kaldes multifunktionelle enzymer.
Klassificering efter medfaktorer
En anden klassifikation er klassificeringen i henhold til kofaktorernes overvejelse. Kofaktorer, coenzymer og co-substrater er navne på forskellige klassifikationer af stoffer, der påvirker biokemiske reaktioner gennem deres interaktion med enzymer.
Organiske molekyler og ioner (for det meste metalioner) betragtes.
De rene proteinenzymer består udelukkende af proteiner, og det aktive centrum er kun dannet af aminosyrerester og peptidrygraden. Aminosyrer er en klasse af organiske forbindelser med mindst en carboxygruppe (-COOH) og en aminogruppe (-NH2).
Holoenzymerne består af en proteinkomponent, apoenzymet og en kofaktor, et molekyle med lav molekylvægt (ikke et protein). Begge sammen er vigtige for enzymets funktion.
Koenzymer
Organiske molekyler som kofaktorer kaldes coenzymer. Hvis de er kovalent bundet til apoenzymet, kaldes de protesegrupper eller co-substrater. En protesegruppe refererer til ikke-proteinkomponenter, der er fast (hovedsageligt kovalent) bundet til et protein med en katalytisk virkning.
Kosubstrater er navne på forskellige klassifikationer af stoffer, der påvirker biokemiske reaktioner gennem deres interaktion med enzymer. Som biokatalysatorer fremskynder molekyler reaktioner i organismer, enzymer fremskynder biokemiske reaktioner. De reducerer aktiveringsenergien, der skal overvindes, så stoffet kan omdannes.